|
Autor:
Ing. Víctor Cires
Gavidia
Octubre, 2003
|
P
|
odemos ponerle una piel metálica a una estatuilla de
plástico, brillante y duro cromo a la defensa de un
automóvil, recuperar "impurezas" de oro y plata del
cobre, para convertirlo en cobre más puro, fabricar
discos fonográficos, ponerle una piel de oro a otros
metales más baratos, darle hermosos colores al
aluminio y aún fabricar metales antes inexistentes,
etc.
|
|
|
Todo esto lo hacemos por medio de la electricidad.
¿No es por lo tanto ésta, una electricidad mágica?
Si colocamos dos placas de cobre en una solución de sulfato de
cobre (CuSO4) y hacemos pasar una corriente, observaremos que
una placa se va engrosando, mientras que la otra se adelgaza.
Este procedimiento se utiliza en las refinerías de cobre para
producir cobre electrolítico, del que utilizamos en nuestros
alambres eléctricos y que debe de tener un grado de pureza mayor
que el 99.9%.
Para ello se utilizan láminas de cobre puro como cátodos, o sean
los electrodos negativos donde se van a depositar los átomos de
cobre que se forman de los iones de cobre de la solución al
recibir sus electrones faltantes.
Los ánodos, o electrodos positivos, son formados por gruesas
placas de cobre impuro, de los que los átomos de cobre van a
pasar a la solución formando más sulfato de cobre y las
"impurezas", oro y plata, entre otras, caen al fondo de las
cubas electrolíticas en forma de lodos para ser recuperadas.
Si en una solución de ácido sulfúrico, colocamos dos placas de
plomo y hacemos pasar la corriente, aunque los químicos no nos
han podido aclarar exactamente todas las reacciones químicas que
suceden, resulta que en una placa se deposita plomo puro y en la
otra se forma una costra de sulfato de plomo.
Si interrumpimos la corriente, observaremos que existe un
voltaje o sea una tensión eléctrica entre los electrodos de
plomo y de sulfato de plomo (la costra que se ha formado sobre
nuestro electrodo negativo)
Gran parte, (no toda) de la energía eléctrica que se utilizó al
hacer pasar corriente por nuestro acumulador, se convirtió en
energía electroquímica, que queda así "cargado", es decir,
convertido en una pila que nos puede proporcionar gran parte de
la energía eléctrica con que lo cargamos.
La razón por la que no toda la energía con que cargamos el
acumulador, se convierte en energía electroquímica, es debido a
que parte se convierte en calor, producido al pasar por los
alambres la corriente con que cargamos la batería, calor que "se
pierde" al ser radiado al espacio, o conducido al aire que rodea
al alambre.
Nuestro proceso no es 100 % eficiente.
Si descargamos totalmente nuestro acumulador, los dos electrodos
quedan cubiertos por una película de sulfato de plomo y la
acción electrolítica se neutraliza, ya no nos produce voltaje.
Como todos los fenómenos químicos se realizan en la superficie,
ha sido de interés aumentar ésta lo más posible, sin aumentar el
tamaño de los acumuladores. Para ello se construyen los
electrodos con un enrejado de plomo: uno de ellos se rellena con
una pasta de litargirio (óxido de plomo) y el otro con una pasta
formada por sesquióxido de plomo y ácido sulfúrico. Con esto se
aumenta considerablemente la capacidad del acumulador. Este tipo
de acumulador ácido, tiene poca resistencia interna y nos puede
producir una corriente muy grande momentáneamente, tal como la
necesitamos por ejemplo en el arranque de un automóvil.
Existen también acumuladores alcalinos, cuya vida es más larga y
que son relativamente más baratos, con los que se fabrican
baterías que se usan donde no son necesarias corrientes
momentáneas muy altas, por ejemplo para la operación de
interruptores en las subestaciones eléctricas o para operación
de lámparas de emergencia.
Veamos ahora otra aplicación de nuestra electricidad química,
Sobre un disco de cera, que se hace girar a velocidad constante,
una aguja de diamante traza surcos separados una fracción de
milímetro, de una misma profundidad. La aguja se hace vibrar,
desplazándola horizontalmente, a la frecuencia producida por
determinado sonido y el surco se convierte en un camino sinuoso
debido a esas vibraciones.
Sobre el disco así "grabado", se coloca una finísima capa de
grafito, que es un material conductor. Se coloca como cátodo en
una cuba electrolítica con un ánodo de plata y un electrólito de
sales de plata. Se hace pasar la corriente y queda nuestro disco
cubierto con una delgada película de plata. Se lleva a una
segunda cuba, donde se repite el procedimiento, pero ahora se
recubre con una gruesa película de cobre.
Así se produce un disco "patrón", que es una imagen del
original, lo que antes eran surcos, son ahora protuberancias.
De este disco patrón, por el mismo procedimiento se obtienen
varias "madres", o sea discos similares al original.
De estas se obtienen varios "positivos", que son los que sirven
para imprimir las copias que se lanzan al mercado.
Como verán, los antiguos discos de 78, 45 ó 33 rpm, eran la
copia de la copia de la copia del original.
Actualmente la música viene empaquetada en "discos compactos",
que utilizan un rayo láser, o en cintas magnéticas, de lo que
platicaremos mas adelante.
El proceso electroquímico nos sirve para reproducir con toda
fidelidad los más mínimos detalles.
Así podemos reproducir monedas o medallas antiguas, fabricar
tipos de imprenta, hacer placas en relieve o grabadas, etc.
También esta electricidad química, nos sirve para hacer
aluminio.
El aluminio, a diferencia de otros metales como el oro, el
cobre, el mercurio, etc, no se encuentra en la naturaleza en su
forma metálica y ha sido en realidad un metal hecho por el
hombre.
Desde fines del siglo dieciocho, químicos como
Lavoisier,
pensaban que la alúmina era el óxido de un metal, el cual no
había podido ser "fabricado" por procedimientos químicos.
Este óxido de aluminio se encuentra en la naturaleza en muy
diversas formas, desde el esmeril y la arcilla, hasta en piedras
preciosas como el zafiro y el rubí.
El primero en producir aluminio metálico fue
Roberto Bunsen en
1854, haciendo pasar una corriente eléctrica en una mezcla de
cloruro de aluminio fundido y sal común, produciéndose cloro y
gotas de aluminio metálico. |
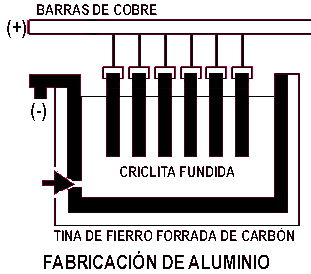 |
Este proceso perfeccionado por Pablo Hérault en Francia y
Carlos Hall en Estados Unidos es el que se utiliza fundamentalmente en
la actualidad.
Alumina purificada, se disuelve en criolita fundida y en esta
solución se hace pasar una gran corriente eléctrica entre
electrodos de carbón, corriente que no sólo sirve para llevar a
cabo el proceso electrolítico, produciendo
aluminio
meta- |
|
lico fundido, que se recoge del fondo de la cuba y oxígeno, que
reacciona con los electrodos de carbón, produciendo óxidos de
carbón, sino que también la corriente eléctrica produce el calor
necesario para tener la solución a 950 grados centígrados,
bastante mayor que la temperatura de fusión del aluminio (659
Grados Centígrados).
El aluminio fundido se extrae del fondo de la cuba y lo que se
gasta, aparte de la gran corriente eléctrica, son los
electrodos de carbón, que se tienen que reemplazar y el mineral
(criolita) que se tiene que estar agregando al electrolito.
La electroquímica es una de tantos territorios casi
inexplorados, en los que pocos se quieren meter, los
electricistas piensan que es territorio de los químicos y éstos,
que es de los electricistas.
De cualquier manera falta mucho por hacer y por investigar.
Algo se ha hecho, por ejemplo las "celdas de energía".
En estas celdas, se ha tratado de producir energía eléctrica
directamente mediante el uso de algún "combustible".
El producir energía eléctrica directamente de la energía
química, se ha tratado de hacer desde fines del siglo pasado.
Fue en 1839 cuando Guillermo Grove tuvo éxito en lograrlo al
fabricar lo que él llamó su batería de gas.
Consiste esta celda, bautizada actualmente con el nombre de "hydrox",
en un recipiente dividido en tres cámaras por medio de dos
paredes intermedias hechas de platino poroso.
La cámara central, limitada por las dos paredes de platino, se
llena con una solución de ácido sulfúrico. En una de las cámaras
laterales se pone a presión hidrógeno y en la otra oxígeno,
también a presión.
Los iones de hidrógeno de la solución (positivos), toman sus
electrones faltantes de los átomos de oxígeno a través de los
poros del platino y forman agua (H2O).
Los iones del radical SO4 (negativos), ceden sus electrones
libres al hidrógeno formando ácido sulfúrico H2SO4.
La reacción se mantiene inyectando oxígeno e hidrógeno a la
celda y produciéndose agua y energía eléctrica entre los
electrodos.
Una versión moderna de esta celda, bautizada con el nombre de "Hydrox",
por J.T.Bacon en Cambridge, consiste en un electrólito de
hidróxido de potasio y electrodos de níquel poroso, opera a 400
grados fahrenheit y a una presión de 400 libras por pulgada
cuadrada.
Esta celda experimental de Bacon, ha producido una potencia de 6
KW (seis mil watts) con una eficiencia de conversión de energía
química en eléctrica superior al 80 %.
Actualmente se experimenta en todo el mundo con tipos de celdas
similares y parece ser que el uso de gases como "combustibles"
son los más prometedores para llegar a producir una celda
económica.
Esto ya se ha logrado (1997) y ya circulan en Chicago autobuses
impulsados por energía proveniente de celdas de combustible
(hidrógeno).
La Mercedes Benz, ya tiene un automóvil experimental operado por
celdas de combustible basadas en un proceso canadiense.
Se espera que para el año 2005 ya circulen automóviles
impulsados por energía proveniente de celdas de combustible que
se cargará en gasolineras como los coches actuales, pero con una
eficiencia del doble de los actuales y sin producir
contaminación. |
|